6-09-1: 放射性崩壊
重要な化学反応は暗記するのと同様に、α、β、γ崩壊は覚えましょう!
※ ページ最上部の(一部スマホでは右上または下側の \(\equiv\) 印「メニュー」をまずクリックしてから)各分野のタイトルをクリックすると、 目次 が見れます。また、スマホは画面を横長にして見ることをおすすめします。
ポイント
・ α崩壊 \(^{A}_{Z}\text{X} →\; \) \(^{4}_{2}\text{He} \) \(+\; ^{A-4}_{Z-2}\text{Y} \) (1)
・ β崩壊 \(^{A}_{Z}\text{X} →\; \) \(e^{-} \) \(+\; ^{A}_{Z+1}\text{Y} \)( \(+\)○ ) (2)
[ ○印は覚えなくてよい ]
・ γ崩壊 \(^{A}_{Z}\text{X} ^*→\; \) \(\gamma\) \(+\; ^{A}_{Z}\text{X} \) (3)
放射性崩壊とは、原子核が粒子線 ―― α線、β線、γ線 ―― を放出する現象のこと。20世紀初めは粒子線の正体がまだ不明だったことから、α、β、γのように名付けられた。
α崩壊では、原子核\(^{A}_{Z}\text{X} \)中から、核子\(p,p,n,n\)4つ分がひとかたまりとなって\(^{4}_{2}\text{He} \)の形で放出される。その際\(^{4}_{2}\text{He} \)は周りに電子を引き連れないので、原子ではなく原子核の状態。よってα線の正体はヘリウム原子核である。崩壊式はポイントの(1)の通り。原子核XからYへと、核子数が4減り、原子番号が2減る。
β崩壊では、原子核中の中性子\(n\)が陽子\(p\)に変換すると同時に電子\(e^{-} \)が放出される。原子物理分野に独特の反応だと理解すればよい。つまりβ線の正体は電子で、特に「高速の電子」と表現したりする。崩壊式はポイント(2)。中性子\(n\)が陽子\(p\)に変換するので、原子核XからYへと核子数は変わらないが、原子番号が1増える。なお詳しく言うと、(2)の右辺で\(e^{-} \)だけでなく、○という素粒子も放出される。名前は反電子ニュートリノで\(\bar{\nu}_e \)と表記するが、これは大学の専門分野の話になるので覚えなくてよい。
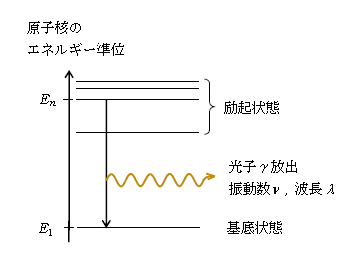
さて、γ崩壊。実は、原子核にも原子同様エネルギー準位がある(6-06-2、図1)。通常原子核はエネルギーの最も低い状態(基底状態)にあって\(^{A}_{Z}\text{X} \)と表記するが、中にはエネルギーの高い状態(励起状態)の原子核もあって、しばしば\(^*\)印付きで\(^{A}_{X}\text{X} ^*\)と表記する。励起状態から基底状態に移るときに、ボーアの振動数条件(6-06-3)
\(\displaystyle h\nu=h\frac{c}{\lambda}=E_n-E_1 \)
に従って光子(\(\gamma\)と表記)が放出される。つまりγ線の正体は光子。原子核のエネルギー準位の差\(E_n-E_1 \)に相当する光子の波長\(\lambda\)は10\(^{-12}\)m程度あるいはもっと短く、よってX線の波長よりも短い。それでγ線を「波長の極めて短い電磁波」と表現したりする。崩壊式はポイント(3)。原子核が励起状態から基底状態に移るだけなので、核子数も原子番号も変わらない。